유
(주)유한양행유한프레가발린서방정75밀리그램(프레가발린)
분류전문의약품 | 기타의 중추신경용약 | 01190
제형-
보험642106010 | 513원/1정
포장30정/상자[6정/PTP X 5]
보관기밀용기, 실온(1~30℃)보관
성분함량
| 프레가발린 | 75.0 mg |
효능효과
성인에서 말초 신경병증성 통증의 치료
용법용량
1. 이 약은 1일 1회, 저녁 식사 후 투여한다. 이 약은 통째로 삼켜야 하며, 쪼개거나 으깨거나 씹어서는 안 된다. 이 약은 주로 신장으로 배설되므로, 신기능이 저하된 환자에 대해서는 용량이 조절되어야 한다(‘2. 신기능 장애 환자’항 참고).
성인: 이 약은 시작용량으로 1일 150 mg 1정을 투여할 수 있다. 개개 환자에서의 반응과 내약성에 근거하여, 일주일 간격으로 1일 최대 600 mg까지 증량할 수 있다.
투여의 중단:
현재의 임상적 경험에 따르면, 이 약의 투여를 중단할 경우, 적어도 1주일 이상의 간격을 두고 점진적으로 중단하여야 한다.
2. 신기능 장애 환자
이 약(프레가발린 75mg)은 중등증 신장애 환자의 시작용량으로만 사용한다.
용량 의존적 이상반응을 고려하였을 때, 프레가발린이 주로 신장으로 배설되므로 신기능이 저하된 환자에서는 용량을 조절한다. 신장애 환자에서의 용량조절은 추정 사구체 여과율(eGFR)에 근거한다[표1].
[표 1] 신기능에 근거한 이 약의 용량 적용
*추정 사구체 여과율(eGFR)은 아래의 MDRD(Modification of Diet in Renal Disease) 공식에 의해 계산할 수 있다.
Scr, std: 혈장 크레아티닌은 표준화된 분석법으로 측정 (mg/dL)
추정 사구체 여과율(eGFR)이 30 mL/min/1.73m2 미만인 중증 신장애 또는 말기 신질환 환자에 대한 이 약의 안전성과 유효성은 확립되지 않았다(사용상의 주의사항 ’12. 전문가를 위한 정보’ 중 ‘(2)약동학적 정보’항 참조).
3. 간기능 장애 환자
이 약은 간기능 장애 환자에서의 안전성과 유효성이 확립되지 않았다.
4. 소아 및 청소년 환자
이 약은 만 19세 미만 소아 및 청소년 환자에서의 안전성과 유효성이 확립되지 않았다.
5. 고령자(만 65세 이상)
이 약은 만 65세 이상의 고령자에서의 안전성과 유효성이 확립되지 않았다.
성인: 이 약은 시작용량으로 1일 150 mg 1정을 투여할 수 있다. 개개 환자에서의 반응과 내약성에 근거하여, 일주일 간격으로 1일 최대 600 mg까지 증량할 수 있다.
투여의 중단:
현재의 임상적 경험에 따르면, 이 약의 투여를 중단할 경우, 적어도 1주일 이상의 간격을 두고 점진적으로 중단하여야 한다.
2. 신기능 장애 환자
이 약(프레가발린 75mg)은 중등증 신장애 환자의 시작용량으로만 사용한다.
용량 의존적 이상반응을 고려하였을 때, 프레가발린이 주로 신장으로 배설되므로 신기능이 저하된 환자에서는 용량을 조절한다. 신장애 환자에서의 용량조절은 추정 사구체 여과율(eGFR)에 근거한다[표1].
[표 1] 신기능에 근거한 이 약의 용량 적용
| 추정 사구체 여과율 (eGFR*, mL/min/1.73m2) |
프레가발린 1일 총 투여량 |
투여방법 |
|
| 시작용량 (mg/일) |
최대용량 (mg/일) |
||
| ≥60 |
150 |
600 |
1일 1회 |
| ≥30-<60 |
75 |
300 |
1일 1회 |
*추정 사구체 여과율(eGFR)은 아래의 MDRD(Modification of Diet in Renal Disease) 공식에 의해 계산할 수 있다.
| eGFR (mL/min/1.73m2)= 175 x (Scr, std)-1.154 x (나이)-0.203 x (0.742 여성의 경우) x (1.212 흑인인 경우) |
Scr, std: 혈장 크레아티닌은 표준화된 분석법으로 측정 (mg/dL)
추정 사구체 여과율(eGFR)이 30 mL/min/1.73m2 미만인 중증 신장애 또는 말기 신질환 환자에 대한 이 약의 안전성과 유효성은 확립되지 않았다(사용상의 주의사항 ’12. 전문가를 위한 정보’ 중 ‘(2)약동학적 정보’항 참조).
3. 간기능 장애 환자
이 약은 간기능 장애 환자에서의 안전성과 유효성이 확립되지 않았다.
4. 소아 및 청소년 환자
이 약은 만 19세 미만 소아 및 청소년 환자에서의 안전성과 유효성이 확립되지 않았다.
5. 고령자(만 65세 이상)
이 약은 만 65세 이상의 고령자에서의 안전성과 유효성이 확립되지 않았다.
사용상 주의사항
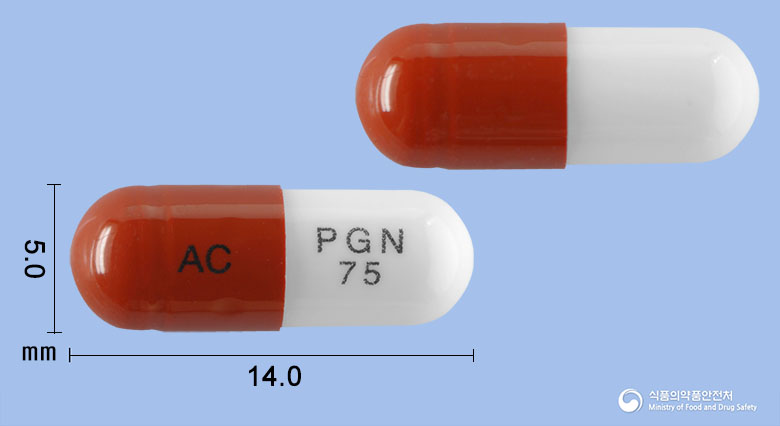
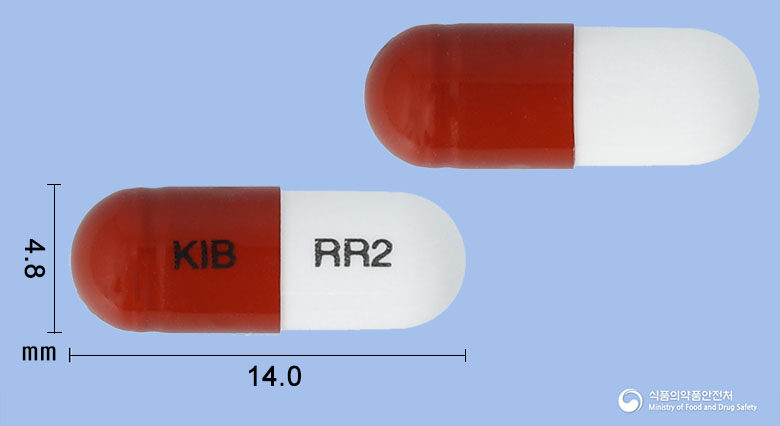
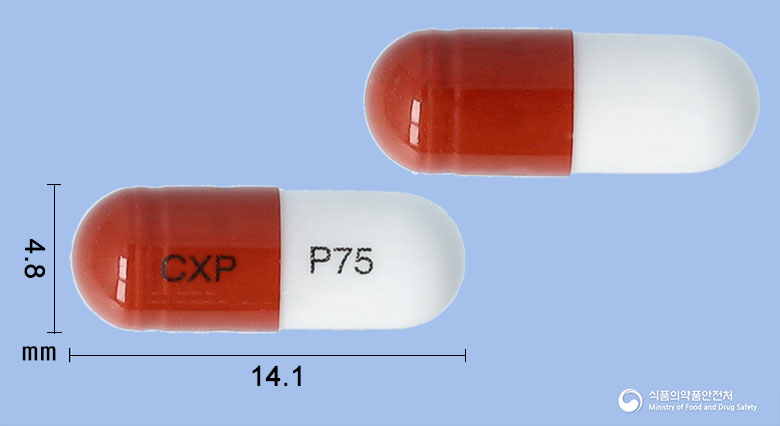
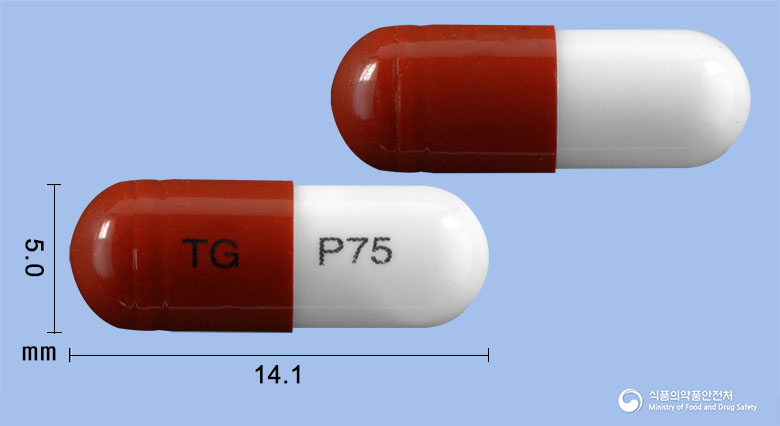
외형정보
성상
연한 살구색의 장방형 필름코팅 서방정
제형
-
모양
타원형
식별표시(앞)
YHP75
식별표시(뒤)
-
크기(mm)
13.7 x 8.0 x 5.2
색상(앞)
분홍
색상(뒤)
-
분할선(앞)
-
분할선(뒤)
-