한
한국화이자제약(주)인라이타정1밀리그램(엑시티닙)
분류전문의약품 | 신약 | 04210
제형-
보험648902130 | 9,990원/1정
포장28정 (14/블리스터X2), 56정 (14/블리스터X4)
보관기밀용기, 실온((15-30℃) 보관
성분함량
| 엑시티닙 | 1.00 mg |
효능효과
1. 진행성 신세포암의 1차 요법
이 약은 펨브롤리주맙과 병용하여 진행성 신세포암의 1차 치료에 사용
2. 진행성 신세포암의 2차 요법
단독요법으로 이전의 한 가지 전신요법에 실패한 진행성 신세포암 치료에 사용
이 약은 펨브롤리주맙과 병용하여 진행성 신세포암의 1차 치료에 사용
2. 진행성 신세포암의 2차 요법
단독요법으로 이전의 한 가지 전신요법에 실패한 진행성 신세포암 치료에 사용
용법용량
이 약의 권장용량은 음식물과 관계없이 5 mg 1일 2회(12시간 간격) 투여로, 매 3주마다 펨브롤리주맙 200 mg을 30분에 걸쳐 정맥점적으로 병용하며, 질환의 진행 또는 허용불가 독성이 발생하기 전까지 투여한다.
이 약과 펨브롤리주맙 병용시, 이 약의 개시용량 5 mg에서의 증량은 6주 이상의 간격으로 고려될 수 있다. 펨브롤리주맙의 권장용량은 펨브롤리주맙의 허가사항을 참고한다.
이 약을 단독요법으로 사용하는 경우, 권장 개시용량은 5 mg 1일 2회 경구 투여이다.
이 약은 음식과 관계없이, 약 12시간 간격으로 복용한다.
이 약은 물과 함께 통째로 삼켜야 한다. 환자가 이 약 복용 후 구토하였거나, 복용을 잊은 경우, 추가 용량을 복용해서는 안 된다. 다음 처방 용량은 기존 복용시간에 그대로 복용해야 한다.
환자 개개인에서의 안전성과 내약성에 근거하여 투여용량의 증량 또는 감량이 권장된다.
치료기간 동안, 적어도 연속 2주간 2등급을 초과하는 이상반응 (이상반응 표준 용어 기준 Common Toxicity Criteria for Adverse Events [CTCAE]에 따름)이 없고, 정상 혈압을 유지하고 있으며, 고혈압 치료제를 복용하지 않는 환자는 용량을 증량할 수 있다. 5 mg 1일 2회 투여에서 증량이 권장되면, 7 mg 1일 2회 투여로 증량 가능하며, 동일한 기준에 따라, 최대 10 mg 1일 2회 투여까지 추가 증량할 수 있다.
치료기간 동안 일부 이상반응의 조절을 위해 이 약 치료의 일시적 또는 영구 중단 및/또는 용량 감량이 필요할 수 있다. 일반적으로, CTCAE 3등급의 이상반응 발생 시, 이 약을 한 단계 낮은 용량으로 감량하며, 4등급 이상반응 발생 시는 이상반응이 2등급 이하로 회복될 때까지 이 약 치료를 일시 중단한 후, 한 단계 낮은 용량에서 재시작한다. 만약 5 mg 1일 2회 투여에서 감량이 필요할 경우, 3 mg 1일 2회 투여로 감량이 권장된다. 만약 추가 감량이 필요할 경우, 2 mg 1일 2회 투여까지 감량할 수 있다.
강력한 CYP3A4/5 저해제 (예, 케토코나졸, 이트라코나졸, 클래리트로마이신, 아타자나비르, 인디나비르, 네파조돈, 넬피나비르, 리토나비르, 사퀴나비르, 텔리트로마이신 및 보리코나졸)와의 병용투여는 피해야 한다. CYP3A4/5 억제 가능성이 없거나, 최소화된 대체 병용 약물의 선택이 권장된다. 강력한 CYP3A4/5 저해제를 투여받는 환자에서 이 약의 용량 조절이 연구된 바는 없으나, 만약 강력한 CYP3A4/5 저해제가 병용 투여 되어야만 하는 경우, 이 약의 용량을 약 절반까지 감량하는 것이 권장된다. 이 감량은 엑시티닙의 AUC (시간-혈장농도 곡선하면적)가 저해제를 병용하지 않았을 때의 범위로 조절될 것으로 예측되는 수준이다. 이후 용량은 환자 개개인의 안전성과 내약성에 근거해 증량하거나 감량할 수 있다. 강력한 CYP3A4/5 저해제의 병용투여가 중지되면, 이 약 투여 용량을 저해제 병용투여 이전으로 변경하여야 한다 (저해제 반감기의 3-5배 시간이 지난 이후). [사용상주의사항 중 ‘ 5. 상호작용’ 참조].
경증 간장애 (Child-Pugh class A) 환자에 대해 이 약의 시작 용량 조절은 필요하지 않다. 약동학 자료에 따라, 베이스라인에서 중등도의 간장애 (Child-Pugh class B) 환자에게는, 이 약의 시작용량을 약 절반으로 감량할 것이 권장된다. 이후 용량은 환자 개개인의 안전성과 내약성에 근거해 증량하거나 감량할 수 있다. 이 약은 중증 간장애 (Child-Pugh class C) 환자에 대해 평가된 바 없다 [사용상주의사항 중 ‘4. 일반적 주의 11) 항’ 참조].
이 약과 펨브롤리주맙을 병용투여하는 환자에서,
• 총 빌리루빈의 정상상한치 2배이상 상승이 없으면서, ALT 또는 AST가 정상상한치의 3배이상에서 10배미만 상승이 있는 경우, 이러한 이상반응이 0 - 1등급으로 회복될 때까지 이 약과 펨브롤리주맙의 투여를 모두 보류한다. 코르티코스테로이드 요법을 고려한다. 회복 후에는 한 가지 약물의 재투여나, 두 가지 약물의 순차적 재투여를 고려한다. 이 약을 재투여하는 경우, 권장용량조절 지침에 따른 용량감소를 고려한다.
• ALT 또는 AST가 정상상한치의 10배이상이거나, 정상상한치의 3배초과이면서 동시에 총 빌리루빈이 정상상한치의 2배이상으로 상승하는 경우, 이 약과 펨브롤리주맙을 모두 영구중단하고, 코르티코스테로이드 요법을 고려한다.
펨브롤리주맙의 추가 용량조절은 펨브롤리주맙 허가사항을 참조한다.
이 약과 펨브롤리주맙 병용시, 이 약의 개시용량 5 mg에서의 증량은 6주 이상의 간격으로 고려될 수 있다. 펨브롤리주맙의 권장용량은 펨브롤리주맙의 허가사항을 참고한다.
이 약을 단독요법으로 사용하는 경우, 권장 개시용량은 5 mg 1일 2회 경구 투여이다.
이 약은 음식과 관계없이, 약 12시간 간격으로 복용한다.
이 약은 물과 함께 통째로 삼켜야 한다. 환자가 이 약 복용 후 구토하였거나, 복용을 잊은 경우, 추가 용량을 복용해서는 안 된다. 다음 처방 용량은 기존 복용시간에 그대로 복용해야 한다.
환자 개개인에서의 안전성과 내약성에 근거하여 투여용량의 증량 또는 감량이 권장된다.
치료기간 동안, 적어도 연속 2주간 2등급을 초과하는 이상반응 (이상반응 표준 용어 기준 Common Toxicity Criteria for Adverse Events [CTCAE]에 따름)이 없고, 정상 혈압을 유지하고 있으며, 고혈압 치료제를 복용하지 않는 환자는 용량을 증량할 수 있다. 5 mg 1일 2회 투여에서 증량이 권장되면, 7 mg 1일 2회 투여로 증량 가능하며, 동일한 기준에 따라, 최대 10 mg 1일 2회 투여까지 추가 증량할 수 있다.
치료기간 동안 일부 이상반응의 조절을 위해 이 약 치료의 일시적 또는 영구 중단 및/또는 용량 감량이 필요할 수 있다. 일반적으로, CTCAE 3등급의 이상반응 발생 시, 이 약을 한 단계 낮은 용량으로 감량하며, 4등급 이상반응 발생 시는 이상반응이 2등급 이하로 회복될 때까지 이 약 치료를 일시 중단한 후, 한 단계 낮은 용량에서 재시작한다. 만약 5 mg 1일 2회 투여에서 감량이 필요할 경우, 3 mg 1일 2회 투여로 감량이 권장된다. 만약 추가 감량이 필요할 경우, 2 mg 1일 2회 투여까지 감량할 수 있다.
강력한 CYP3A4/5 저해제 (예, 케토코나졸, 이트라코나졸, 클래리트로마이신, 아타자나비르, 인디나비르, 네파조돈, 넬피나비르, 리토나비르, 사퀴나비르, 텔리트로마이신 및 보리코나졸)와의 병용투여는 피해야 한다. CYP3A4/5 억제 가능성이 없거나, 최소화된 대체 병용 약물의 선택이 권장된다. 강력한 CYP3A4/5 저해제를 투여받는 환자에서 이 약의 용량 조절이 연구된 바는 없으나, 만약 강력한 CYP3A4/5 저해제가 병용 투여 되어야만 하는 경우, 이 약의 용량을 약 절반까지 감량하는 것이 권장된다. 이 감량은 엑시티닙의 AUC (시간-혈장농도 곡선하면적)가 저해제를 병용하지 않았을 때의 범위로 조절될 것으로 예측되는 수준이다. 이후 용량은 환자 개개인의 안전성과 내약성에 근거해 증량하거나 감량할 수 있다. 강력한 CYP3A4/5 저해제의 병용투여가 중지되면, 이 약 투여 용량을 저해제 병용투여 이전으로 변경하여야 한다 (저해제 반감기의 3-5배 시간이 지난 이후). [사용상주의사항 중 ‘ 5. 상호작용’ 참조].
경증 간장애 (Child-Pugh class A) 환자에 대해 이 약의 시작 용량 조절은 필요하지 않다. 약동학 자료에 따라, 베이스라인에서 중등도의 간장애 (Child-Pugh class B) 환자에게는, 이 약의 시작용량을 약 절반으로 감량할 것이 권장된다. 이후 용량은 환자 개개인의 안전성과 내약성에 근거해 증량하거나 감량할 수 있다. 이 약은 중증 간장애 (Child-Pugh class C) 환자에 대해 평가된 바 없다 [사용상주의사항 중 ‘4. 일반적 주의 11) 항’ 참조].
이 약과 펨브롤리주맙을 병용투여하는 환자에서,
• 총 빌리루빈의 정상상한치 2배이상 상승이 없으면서, ALT 또는 AST가 정상상한치의 3배이상에서 10배미만 상승이 있는 경우, 이러한 이상반응이 0 - 1등급으로 회복될 때까지 이 약과 펨브롤리주맙의 투여를 모두 보류한다. 코르티코스테로이드 요법을 고려한다. 회복 후에는 한 가지 약물의 재투여나, 두 가지 약물의 순차적 재투여를 고려한다. 이 약을 재투여하는 경우, 권장용량조절 지침에 따른 용량감소를 고려한다.
• ALT 또는 AST가 정상상한치의 10배이상이거나, 정상상한치의 3배초과이면서 동시에 총 빌리루빈이 정상상한치의 2배이상으로 상승하는 경우, 이 약과 펨브롤리주맙을 모두 영구중단하고, 코르티코스테로이드 요법을 고려한다.
펨브롤리주맙의 추가 용량조절은 펨브롤리주맙 허가사항을 참조한다.
사용상 주의사항
외형정보
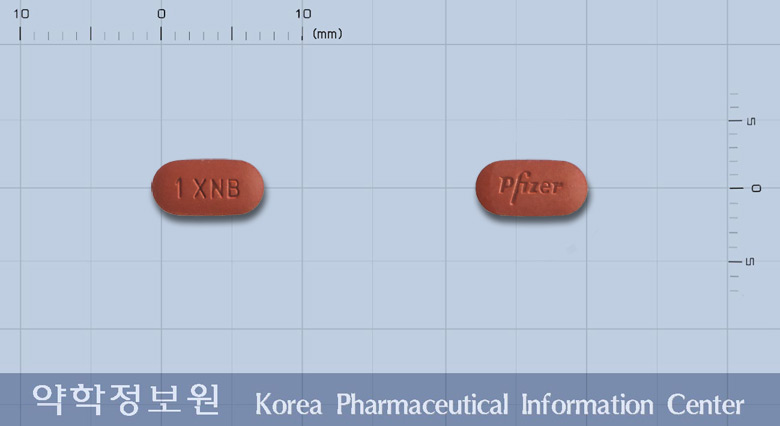
성상
빨간색 타원형모양의 필름코팅정제
제형
-
모양
타원형
식별표시(앞)
1 XNB
식별표시(뒤)
마크
크기(mm)
8.75 x 4.45 x 2.7
색상(앞)
빨강
색상(뒤)
-
분할선(앞)
-
분할선(뒤)
-